2025.11.28
2025年11月24日晚,由深圳湾实验室科技基金会主办的“科研向善者说”公益讲座“罕路同行”系列第一期线上直播如期举行。深圳湾实验室特聘研究员陈南鹏博士以“非对称细胞分裂与杜氏肌营养不良症(Duchenne Muscular Dystrophy,DMD)”为主题,为患者家庭带来了一场专业且易懂的科普讲座,从生物学家的视角为这一罕见病的致病机制、研究进展与治疗方向作了全方位解读。
机制解读:DMD 的致病机制与疾病特点
DMD的核心症结,出在一个“特殊基因”上。陈博士介绍,DMD由X染色体上的“抗肌萎蛋白基因”突变引发——该基因是人类基因组中最大的基因,含超过 250 万个碱基对,拥有79个外显子,编码的抗肌萎蛋白由约3700个氨基酸构成。此外,抗肌萎蛋白在进化中高度保守,最早出现于腔肠动物门,从软体动物、昆虫到脊椎动物再到哺乳动物,演化历程中始终存在,且维持正常功能的保守区域集中在蛋白两端。
抗肌萎蛋白的关键作用,是作为“桥梁”参与构成“抗肌萎蛋白-糖蛋白复合物(DGC)”:该复合物一头连接肌肉细胞表面的受体,一头锚定细胞内的肌动蛋白骨架,能牢牢把肌肉细胞“黏”在细胞外基质上,就像庄稼的根扎在土壤里。一旦抗肌萎蛋白基因突变,这道“桥梁”就会断裂——肌肉细胞失去黏附,如同庄稼脱离土壤,最终逐渐萎缩,引发疾病。
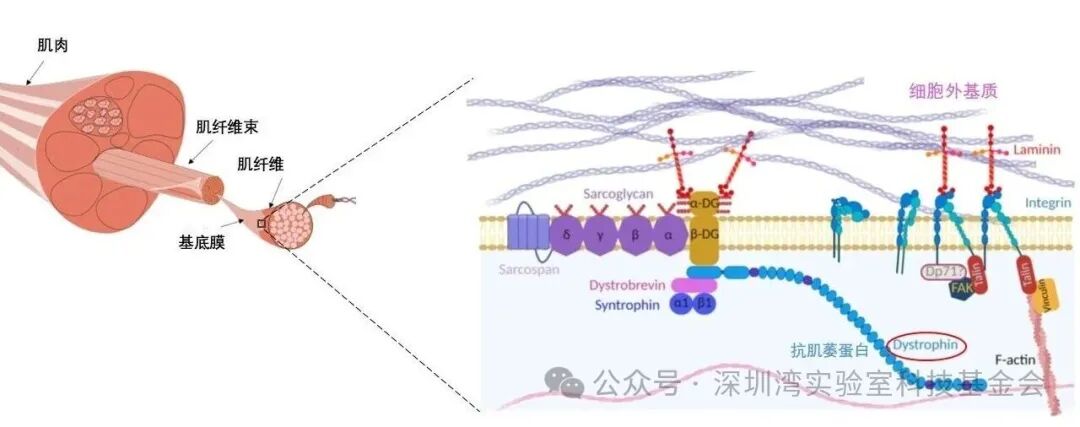
图1,抗肌萎蛋白-糖蛋白复合物(Dystrophin Glycoprotein Complex,DGC):介导肌肉蛋白与细胞外基质黏附的关键复合物
值得注意的是,与DMD“同源”的还有贝氏肌营养不良症(BMD),二者均由抗肌萎蛋白缺陷导致,但症状差异显著:DMD患者多在 2-5 岁发病,12 岁左右丧失行走能力,因蛋白一端结构缺失导致功能完全失效;BMD患者仅蛋白中间区域缩短,两端功能保留,症状更轻微。目前,DMD的诊断已较为成熟,通过肌酶检测、血清指标分析和肌肉活力检测等手段就能明确病情。由于X 染色体连锁遗传特性,该病在新生男孩中的发病率约为 1/3500,男孩患病概率远高于女孩。
研究支撑:动物模型与基础研究突破
要破解DMD,离不开动物模型的“助攻”。陈博士详细介绍了当前研究中常用的“模型团队”:
- 斑马鱼:繁殖快、数量多,适合大规模筛选,但进化距离远,难模拟长期系统性病变;
- 小鼠:遗传背景清晰,实验结果稳定,但DMD小鼠症状轻微(存活至正常寿命 80%),难复现人类重症;
- 金毛猎犬:临床表现最接近人类,但成本高,存在伦理争议,个体间病情差异大;
- 恒河猴:生理、免疫与人类相似度最高(临床前研究金标准),但成本极高,难获取统一遗传背景品系。

图2,DMD的疾病研究动物模型
在解码DMD的道路上,国内研究也取得了关键突破:西湖大学去年解析出DGC复合物的冷冻电镜结构,颠覆了“膜蛋白平行排列”的传统认知,发现DGC实际是高度复合的、相互缠绕的塔状结构;昆明理工大学与中科院昆明动物所则首创DMD恒河猴模型,精准复现人类DMD的症状,为后续机制研究与药物研发提供了关键支撑。
治疗现状:对症缓解为主
目前,DMD尚无根治手段,常规治疗以“对症缓解”为主——使用糖皮质激素抑制肌肉损伤引发的炎症,但长期使用会带来体重增加、向心性肥胖等副作用。
基因疗法是当前的研发热点,但面临一个核心难题:抗肌萎蛋白基因太大,难以通过病毒载体高效递送到肌肉细胞中。2024年7月,FDA 批准了一款针对DMD的基因治疗药物,通过病毒载体递送“缩小版”抗肌萎蛋白基因,帮助患者产生有功能的蛋白,但后续出现两例患者因肝衰竭死亡的案例。
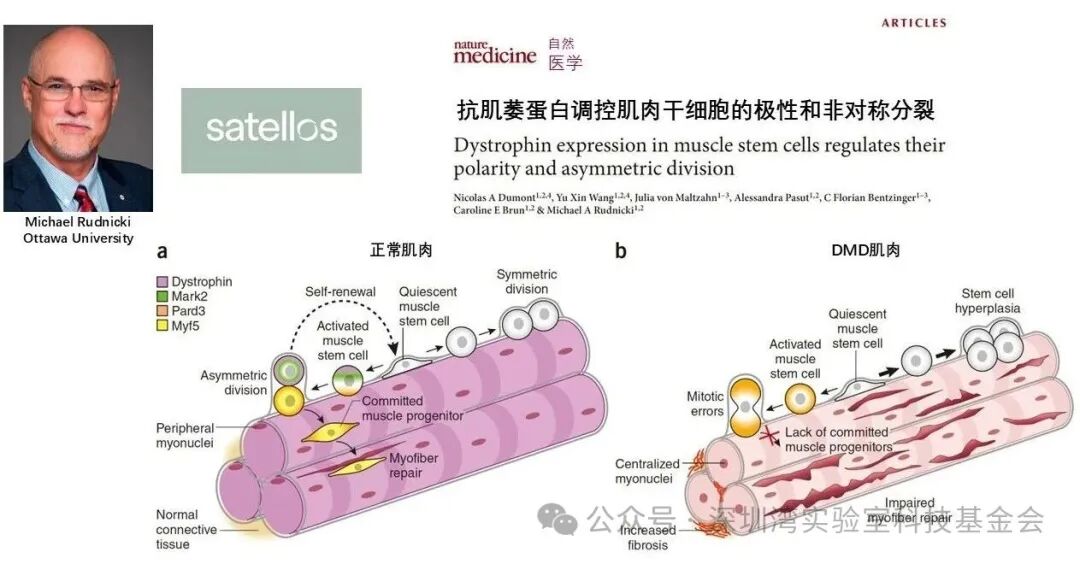
图3,DMD非对称分裂失控-来自小鼠的证据
前沿探索:非对称细胞分裂的关键作用
更具潜力的前沿方向,聚焦于“肌肉卫星干细胞的非对称分裂”。陈博士解释,卫星干细胞是肌纤维的“修复主力”:正常情况下,它会通过“非对称分裂”产生两个子细胞——一个保留干细胞特性(维持储备),一个分化为肌纤维细胞(修复损伤),从而实现“修复不耗竭”。但DMD患者中,这一分裂机制失控,卫星干细胞仅能“对称分裂”产生两个分化细胞,导致干细胞逐渐耗尽,肌肉失去持续再生能力。加拿大Satellos公司已基于这一机制开展临床试验,国内相关研究也在推进,这可能是从根源上缓解DMD的关键方向。
答疑环节:聚焦核心关切
讲座的答疑环节,陈博士针对患者家庭最关心的治疗选择、药物潜力等问题,结合研究进展给出了清晰解答:
• 瓶刷聚合物:这类化学分子可以减轻细胞膜损伤,目前仅在DMD小鼠模型中完成初步验证,能显著抑制肌酸激酶释放(肌肉损伤的关键指标),但仍处于基础研究阶段,尚未进入临床阶段。
• AAV疗法与ASO疗法:两者适用场景不同——AAV 疗法借助病毒载体递送基因,感染肌肉细胞效率高,但受抗肌萎蛋白基因体积大的限制,仅能递送“缩小版”基因;ASO 疗法(反义寡核苷酸疗法)针对性更强,仅适用于特定突变类型患者(如部分外显子缺失或点突变),需结合基因检测结果判断是否适用。
• 干细胞项目差异:国内医院(如苏州大学附属医院、瑞金医院等)的干细胞项目多为临床研究,核心是探索干细胞移植的治疗效果与安全性;而陈博士团队的研究聚焦细胞生物学基础机制,旨在揭示肌肉卫星干细胞非对称分裂的调控逻辑,为干细胞治疗提供靶点支撑,二者处于“临床应用探索”与“基础机制攻关”的不同研究层面。
• 药物潜力:针对肌肉卫星干细胞非对称分裂的药物(如加拿大Satellos公司开发的针对AAK1酶的抑制剂),有充足的基础研究数据支撑,核心优势是有望从根源改善肌肉再生能力,延缓甚至缓解DMD病程,但需经过更多动物实验与临床试验验证,才能明确其在人体中的安全性与有效性。
• 成人治疗:18 岁以上患者的规范治疗需咨询专业医疗机构,建议关注罕见病诊疗协作网络。
• 其他肌营养不良症:肢带型肌营养不良症(如2b型)源于糖蛋白糖基化相关酶的突变(该蛋白仅为抗肌萎蛋白的1/10大小),致病基因和核心病理与DMD存在差异。目前拜耳公司针对这类疾病的AAV基因疗法已进入临床跟踪阶段,安全性表现良好,未来可持续关注相关研究进展。
讲座最后,陈博士引用法国生物学家路易斯・巴斯德的名言:“科学是树,应用则是结在树上的果实”,强调基础研究对疾病治疗的核心价值。他表示,生物学家对DMD致病机制的探索,正是解开治疗难题的核心钥匙,终将为临床治疗提供更精准的思路与方向。
本次直播不仅为患者家庭梳理了DMD的科学认知框架,更传递了“科研向善”的理念。后续“科研向善者说”系列将继续聚焦罕见病相关研究进展,为科研人员、医护人员与患者家庭搭建更多沟通桥梁,让“罕路同行”不再孤单。
欢迎在文末留言分享您的感悟与疑问,我们将持续关注DMD领域科研进展。敬请关注本基金会微信公众号,获取更多公益讲座信息。
撰稿 | 陈南鹏课题组
编辑 | 骑行悟空